RIES
Research Institute for Electronic Science, Hokkaido University
北海道大学
電子科学研究所

LAST UPDATE 2017/02/25
-
研究者氏名
Researcher Name佐藤勝彦 Katsuhiko SATO
准教授 Associate Professor -
所属
Professional Affiliation北海道大学電子科学研究所
知能数理研究分野
Research Institute for Electronic Science, Hokkaido University
Mathematical and Physical Ethology Lab. -
研究キーワード
Research Keywords形態形成
数理モデル
連続体力学
縮約
morphogenesis
mathematical modeling for complex phenomena in biology
continuum mechanics
reductive perturbation to dynamical systems
- 研究テーマ
Research Subject -
生命現象への力学的アプローチ
Mechanical approaches to biological systems
研究の背景 Background
DNAの発見以来、生物は化学反応の集合体として捉えられ、大きな成功を収めてきてますが、近年、生物の形成には化学反応だけではなく、力学的な相互作用(力)が重要な役割を果たしていることが明らかになってきています。たとえば心臓などのような構造がある組織を作るときには細胞間の反応拡散的な相互作用だけではなく、各細胞は収縮力を出してお互いの硬さや力学的応答を得ることによって細胞の分化や形態形成がなされると考えられています。生物の理解には、化学反応の視点とともに力学的なアプローチ(弾性論、粘弾性理論、力学的数理モデル)が必要となってきています。
Since the discovery of DNA double helix, biological systems have been regarded as complex chemical reaction systems and much progress in understandings of it has been achieved. However, recently, many investigators have recognized that mechanical interactions between fundamental components of the biological systems, such as cells and microfilaments of actin, also play an important role in the formation of biological systems. To understand biological systems more completely, we need to take mechanical notions developed in physics into biology
研究の目標 Outcome
生物における力の役割を捉えるために各階層で現れる非自明な現象に注目して、化学反応だけでなく力学的な視点から数理モデルを構築して、その現象の本質を抽出することを目標としています。具体的には、組織・器官の階層では上皮細胞の集団運動を扱って、細胞が何故隣の細胞とくっついたまま動くことができるのかについて答えます。細胞の階層では筋肉の自励振動に注目して、力によって相互作用する素子の複雑な振る舞いの出所を調べます。ミクロな階層ではアクチン・ミオシンのネットワークのダイナミックスに注目して、自発的に形成されるパターンについて調べます。これらを行うことによって、生命現象でのミクロからマクロまでの包括的な理解が期待できます。
We extract essences of interesting phenomena appearing in biological systems by constructing some mathematical models based not only on chemical reactions but also on mechanical principles. To be specific, at the tissue level, we focus on collective migration of epithelial cells, and ask why they can move keeping their attachment with adjacent cells. At the cellular level, we focus on auto-oscillations in muscle, and ask what is the essence of various complex oscillation patterns. At the actomyosin level, we focus on their spontaneous formation of mesoscopic structures due to the flow.
研究図Research Figure
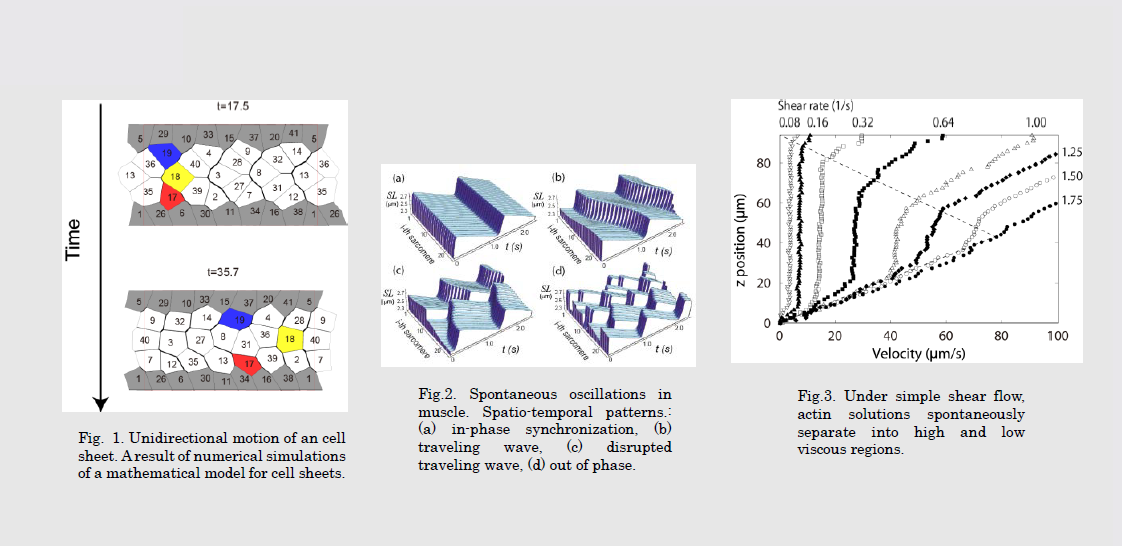
文献 / Publications
Phys. Rev. Lett. 111 108104 (2013). Phys. Rev. Lett. 109 248303 (2012). Prog. Biophys. Mol. Biol, 105 199-207 (2011). Europhys. Lett. 94 68004 (2011).
研究者HP
- katsuhiko_sato
 es.hokudai.ac.jp
es.hokudai.ac.jp - http://pel.es.hokudai.ac.jp/